Dioxid de carbon
| Dioxid de carbon | |
 | |
 | |
 | |
| Nume IUPAC | Dioxid de carbon |
|---|---|
| Alte denumiri | Anhidridă carbonică |
| Identificare | |
SMILES C(=O)=O[1]  | |
| Număr CAS | 124-38-9 |
| ChEMBL | CHEMBL1231871 |
| PubChem CID | 280 |
| Informații generale | |
| Formulă chimică | CO2 |
| Aspect | gaz incolor, inodor |
| Masă molară | 44,0099 g/mol |
| Proprietăți | |
| Densitate | 1,9767 kg/m3 (0 °C, 1013 mbar) |
| Starea de agregare | gaz |
| Punct de topire | –56,6 °C (5,3 bar) |
| Punct de fierbere | –78,5 °C (Sublimare) |
| Solubilitate | 3,3 g/l la 0 °C, 1,7 g/l la 20 °C, la 1013 hPa |
| Presiune de vapori | 57,258 bar(20 °C) |
| Fraze S | S9, S23 |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
Modifică date / text  | |

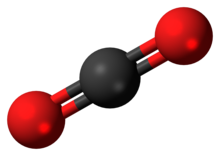
Dioxidul de carbon, format dintr-un atom de carbon și doi atomi de oxigen, este o anhidridă labilă a acidului carbonic (CO2.H2O ~ H2CO3), un compus chimic rezultat din oxidarea carbonului, în majoritate de origine organică. Pe de altă parte, este un produs secundar în procese industriale, cum ar fi producția de ciment, oțel, amoniac, metanol, etilena, acid acetic, acid acrilic și alți compuși organici. Pentru a reduce emisiile nete, este esențial creșterea eficienței proceselor chimice[2][3] și, pe de altă parte, captarea și transformarea a CO2 în combustibili[4][5] și compuși organici[6][7][8][9].
Prezent în atmosferă în concentrația de circa 0,04 %, este strict necesar pentru păstrarea echilibrului biosferei.
Descriere. Proprietăți fizice și chimice
Dioxidul de carbon este un gaz incolor, prezent și în atmosfera terestră în concentrație de aproximativ 0,04 %. Este unul din cele mai importante gaze cu efect de seră[necesită citare].
Formula chimică: CO2.
Echivalent CO2
Termenul de echivalent CO2 desemnează potențialul de încălzire globală al unui gaz, calculat prin echivalența cu o cantitate de dioxid de carbon care ar avea același potențial de încălzire globală, la o anumită scală de timp, de obicei 100 de ani. Dioxidul de carbon este luat ca referință.
Rol fiziologic
Este produs de catabolism al organismelor aerobe. Este transportat de sângele organismelor superioare ca bicarbonat de sodiu, iar sub forma compușilor carbaminici cu hemoglobina de către eritrocite.
Ciclul biologic al carbonului
Procesul de ardere
Substanța organică se oxidează (ardere completă) printr-o reacție exotermă terminată cu degajarea de energie (căldură), dioxid de carbon și apă la oxidarea monomerilor, sau polimerilor de zahăr și de grăsimi, iar la alte substanțe organice, oxizi de metale etc.
Glucoză: C6H12O6 + 6O2 → 6CO2 + 6H2O + energie (Q)
Energia (căldura) poate fi eliberată :
- în timp scurt și la temperaturi înalte, în cazul arderii simple;
- lent și treptat, prin procese biochimice catabolice, care au loc pe toată biosfera, ca bază a metabolismului, de la microb la animal, cu eliminări dozate și controlate de energie/temperatură (spre exemplu, glicoliza, arderea unei hexoze — zahăr cu 6 atomi de carbon — pe calea Embden-Meyerhoff-Parnas (engleză :Embden-Meyerhoff-Parnas pathway) prin ruperea enzimatică a hexozei care duce într-un prim stadiu la piruvat, energia fiind preluată de cofactori: adenozindifosfat ADP care se transformă în adenozintrifosfat ATP și NAD -->NADH; piruvatul, se va descompune enzimatic (ciclul Krebs) la dioxid de carbon, eliminat prin respirație și apă).[10][11][12]
Dioxidul de carbon din atmosferă este preluat de plantele, algele și protozoarele care conțin clorofilă - sau sisteme enzimatice surori - care, împreună cu apa și energia solară resintetizează polimeri zaharide: amidonul, lignina etc.
CO2
- Formula chimică:
- Carbon: nemetal NA: 6 MA: 12,01 Capacitatea combinătoare - 4 y:4
- Oxigen: nemetal NA: 8 MA: 15,99 Capacitatea combinatoare + 2 y:6
- unde NA este numărul atomic, iar MA este masa atomică.
- E: Electroni x[2] (primul nivel), y (al doilea nivel), z (al treilea nivel).
- Are densitatea 1,98 kg/m3N
Note
- ^ „Dioxid de carbon”, carbon dioxide (în engleză), PubChem, accesat în
- ^ Kinetic studies of propane oxidation on Mo and V based mixed oxide catalysts (PDF). .
- ^ „The reaction network in propane oxidation over phase-pure MoVTeNb M1 oxide catalysts”. Journal of Catalysis. 311: 369–385. .
- ^ de Araujo, Gabriel E.; de Castro, Jéssica H.; Monteiro, Wesley F.; de Lima, Jeane; Ligabue, Rosane A.; Lourega, Rogerio V. (), „Methanation of CO2 from flue gas: experimental study on the impact of pollutants”, Reaction Kinetics, Mechanisms and Catalysis (în engleză), 134 (2), pp. 743–757, doi:10.1007/s11144-021-02092-8, ISSN 1878-5204, accesat în
- ^ Chatzilias, Christos; Martino, Eftychia; Katsaounis, Alexandros; Vayenas, Constantinos G. (), „Electrochemical promotion of CO2 hydrogenation in a monolithic electrochemically promoted reactor (MEPR)”, Applied Catalysis B: Environmental (în engleză), 284, p. 119695, doi:10.1016/j.apcatb.2020.119695, ISSN 0926-3373, accesat în
- ^ Regenerative Synthese von chemischen Energiespeichern und Feinchemikalien, accesat în
- ^ „CO2 from the air as a raw material for chemicals” (în engleză). www.biooekonomie-bw.de. Accesat în .
- ^ Torquato, Lilian D. Moura; Pastrian, Fabián A. C.; Perini, João A. Lima; Irikura, Kallyni; de L. Batista, Ana Paula; de Oliveira-Filho, Antonio G. S.; Córdoba de Torresi, Susana I.; Zanoni, Maria V. Boldrin (), „Relation between the nature of the surface facets and the reactivity of Cu2O nanostructures anchored on TiO2NT@PDA electrodes in the photoelectrocatalytic conversion of CO2 to methanol”, Applied Catalysis B: Environmental (în engleză), 261, p. 118221, doi:10.1016/j.apcatb.2019.118221, ISSN 0926-3373, accesat în
- ^ Bonura, G.; Todaro, S.; Frusteri, L.; Majchrzak-Kucęba, I.; Wawrzyńczak, D.; Pászti, Z.; Tálas, E.; Tompos, A.; Ferenc, L. (), „Inside the reaction mechanism of direct CO2 conversion to DME over zeolite-based hybrid catalysts”, Applied Catalysis B: Environmental (în engleză), 294, p. 120255, doi:10.1016/j.apcatb.2021.120255, ISSN 0926-3373, accesat în
- ^ en Bodner, George M.: Metabolism Part I: Glycolysis for the Embden-Meyerhoff pathway, J. Chem. Educ., 1986, 63 (7), p 566, July 1986
- ^ en Curs de Biochimie la Univ. Cornell: Fermentation : A BioMi 290/291 MicroWeb Movie Page, http://courses.cit.cornell.edu/biomi290/MOVIES/GLYCOLYSIS.HTML
- ^ en Engelking, Larry Rex: Textbook of veterinary physiological chemistry, chap. 24, p.137, 2004.
Bibliografie
- en Seppänen, O. A.; Fisk, W. J.; Mendell, M. J. (decembrie 1999). „Association of Ventilation Rates and CO2 Concentrations with Health and Other Responses in Commercial and Institutional Buildings” (PDF). Indoor Air. 9 (4): 226–252. doi:10.1111/j.1600-0668.1999.00003.x. Arhivat din original (PDF) la .
- en Shendell, D. G.; Prill, R.; Fisk, W. J.; Apte, M. G.; Blake, D.; Faulkner, D. (octombrie 2004). „Associations between classroom CO2 concentrations and student attendance in Washington and Idaho” (PDF). Indoor Air. 14 (5): 333–341. doi:10.1111/j.1600-0668.2004.00251.x. Arhivat din original (PDF) la .
- en Soentgen, Jens (februarie 2014). „Hot air: The science and politics of CO2”. Global Environment. 7 (1): 134–171. doi:10.3197/197337314X13927191904925.
- en Good plant design and operation for onshore carbon capture installations and onshore pipelines: a recommended practice guidance document. Global CCS Institute. Energy Institute and Global Carbon Capture and Storage Institute. . Arhivat din original la . Accesat în .
This new title is an essential guide for engineers, managers, procurement specialists and designers working on global carbon capture and storage projects.
Vezi și
Legături externe
- Adrian Sorin Mihalache, Dioxidul de carbon, otrava de pe reversul strălucirii civilizației noastre, Ziarul Lumina, 11 octombrie 2009
| ||||||||||||||||||||||||||||||||||||||










