Oxid de calciu
| Oxid de calciu | |
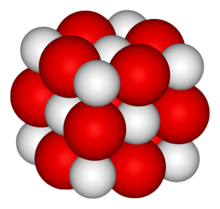 Formula structurală | |
 | |
| Denumiri | |
|---|---|
| Alte denumiri | Var nestins, var calcinat |
| Identificare | |
SMILES O=[Ca][1]  | |
| Număr CAS | 1305-78-8 |
| ChEMBL | CHEMBL2104397 |
| PubChem CID | 14778 |
| Informații generale | |
| Formulă chimică | CaO |
| Aspect | pulbere de culoare albă |
| Masă molară | 56,08 g/mol |
| Proprietăți | |
| Densitate | 3,37 g/cm3 (20 °C) |
| Starea de agregare | solidă |
| Punct de topire | 2570-2580 °C |
| Punct de fierbere | 2850 °C (100 mbar) |
| Solubilitate | greu solubil în apă, 1,65 g/l (la 20 °C), cu reacție exotermică, deoarece se formează hidroxid de calciu |
| Miros | miros de calcar |
| Presiune de vapori | 0 millimetre of mercury[2]  |
 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
Modifică date / text  | |
Oxidul de calciu (varul nestins, varul ars) se prezintă sub formă de pulbere de culoare albă, care cu apa reacționează energic, efervescent cu degajare de căldură formându-se hidroxid de calciu (varul stins).
- CaO + H2O --> Ca(OH)2
Obținere
Oxidul de calciu se obține prin tratarea termică (arderea) la peste 825 °C a pietrei de var (calcar sau carbonat de calciu) cu eliberare de dioxid de carbon:
- CaCO3 --> CaO + CO2
Oxidul calcic este instabil, iar la răcire poate capta dioxid de carbon din aer care după un interval de timp reface carbonatul calcic inițial. Oxidul calcic are o mare afinitate pentru apă și este un desicant mai puternic decât silicagel.
Formarea hidroxidului calcic
Acest proces are o serie de trepte de stingere cu apă a varului nestins după durata timpului de contact cu apa:
- < 2 min var stins puțin
- 2 - 6 min var stins mijlociu
- > 6 min var stins tare
Varul nestins și cel stins (hidroxid de calciu) sunt caustici, având o reacție puternic alcalină (valoare pH 12–13), astfel că se impune evitarea contactului cu pielea și cu ochii.
Formarea carbidului
Varul nestins reacționează cu grafitul într-un cuptor cu arc electric la aproximativ 2200 ° C pentru a forma carbid.
CaO + 3C → CaC2 + CO
Temperatura ridicată necesară pentru această reacție nu este practic realizabilă prin arderea tradițională, astfel încât reacția este efectuată într-un cuptor cu arc electric cu electrozi de grafit. Produsul carbură în general conține aproximativ 80% carbură de calciu în greutate.
Utilizare
Varul nestins este folosit în industria de construcții, la prepararea mortarului pentru tencuială, ca ghips, sau la văruirea pereților, în industria de fabricare a cimentului, la producerea amendamentelor de îmbunătățire a solurilor acide, la producerea acetilurii de calciu. În metalurgie este folosit la desulfurarea minereului de fier. De asemenea este folosit la reținerea sulfului din fum (detoxificare), la obținerea hipocloritului de calciu, sau ca regulator al valorii pH (quantum satis) la alimente (E 529).
Bibliografie
- Linus Pauling, Chimie generală, Editura Științifică, București, 1972 (traducere din limba engleză)
| ||||||||||||||||||||||||||||||||||||||











