Borat
Termenul de borat face referire la un număr mare de oxianioni ai borului și de asemenea la compușii chimici care conțin acești anioni. Compușii cu structuri mai mari conțin geometrii moleculare de tipul trigonal-planare, BO3, sau tetraedrice, BO4, acestea fiind legate prin intermediul atomilor de oxigen[1]. Structurile pot fi ciclice sau liniare. În natură, borul este adesea răspândit sub formă de borați sau borosilicați.
Structuri
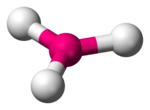
Cel mai simplu anion borat, ionul ortoborat (3-) , [BO3]3-, este cunoscut în stare solidă, cum ar fi de exemplu ortoboratul de calciu, Ca3(BO3)2.[2] Acest ion adoptă o structură aproximativ trigonal-planară, analoagă anionului carbonat, [CO3]2-, cu care este și izoelectronic.
Mineral
Esteri borați

Esterii borați sunt compuși organici care pot fi preparați în urma unei reacții de condensare a acidului boric cu alcoolii. Există două clase de astfel de esteri: ortoborații, B(OR)3 și metaborații, B3O3(OR)3.
- B(OH)3 + 3ROH → B(OR)3 + 3H2O
- 3B(OH)3 + 3ROH → B3O3(OR)3 + 6H2O
Un agent de deshidratare, precum este acidul sulfuric concentrat, este adăugat de obicei în mediul de reacție.[3] Esterii borați sunt compuși volatili și pot fi purificați prin distilare. Această procedură este folosită pentru analiza de urme a boraților și pentru analiza borului în oțel.[4] De asemenea, asemănător tuturor compușilor borului, borații de alchil ard cu o flacără caracteristică verde. Această proprietate este folositoare în determinarea prezenței borului în analiza calitativă.[5]
Vezi și
- Borax
Referințe
- ^ Egon Wiberg, Arnold Frederick Holleman (2001) Inorganic Chemistry, Elsevier ISBN: 0-12-352651-5
- ^ Vegas, A. (). „New description of the Ca3(BO3)2 structure”. Acta Crystallographica Section C. 41 (11): 1689–1690. doi:10.1107/S0108270185009052. ISSN 0108-2701.
- ^ Brown, Herbert C.; Mead, Edward J.; Shoaf, Charles J. (). „Convenient Procedures for the Preparation of Alkyl Borate Esters”. J. Am. Chem. Soc. 78 (15): 3613–3614. doi:10.1021/ja01596a015.
- ^ Mendham, J.; Denney, R. C.; Barnes, J. D.; Thomas, M. J. K. (2000), Vogel's Quantitative Chemical Analysis (6th ed.), New York: Prentice Hall, p. 666, ISBN 0-582-22628-7
- ^ Vogel, Arthur I.; Svehla, G. (1979), Vogel's Textbook of Macro and Semimicro Qualitative Inorganic Analysis (5th ed.), London: Longman, ISBN 0-582-44367-9
| ||||||||||||||||||||||||||||||||











